다광자 이미징
지난 20년 동안 바이오 이미징은 펨토초, 초고속 레이저 기술이 널리 사용되면서 혜택을 보았습니다. 펨토초(10 -15 s)와 피코초(10 -12 s) 펄스는 바이오 샘플에 고유한 물리적 프로세스를 유도하여 기존의 공초점 이미징을 통해서는 볼 수 없는 귀중한 자료를 얻을 수 있게 합니다. 기존의 공초점 이미징이 아닌 다광자 이미징을 선택하는 주된 이유는 뇌 조직과 같은 불투명한 샘플을 더 깊이 영상화할 수 있기 때문입니다. 이것이 어떻게 가능하며, 성공적인 다광자 이미징 실험에 필요한 조건은 무엇일까요?
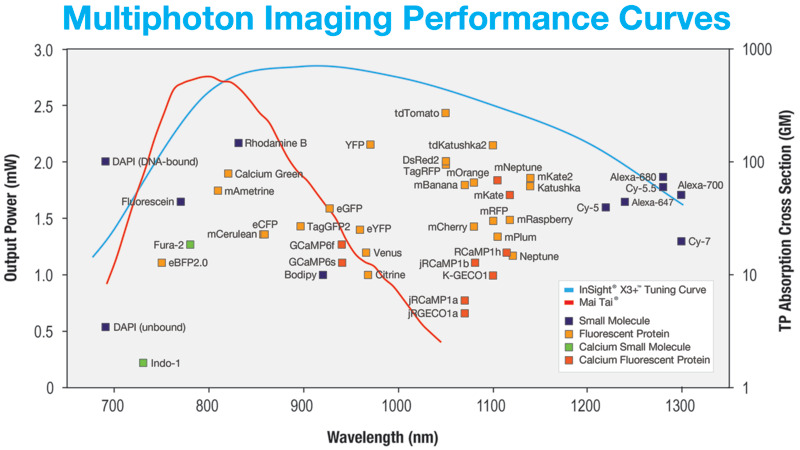
다광자 이미징은 다양한 형광 염료에서 두 개 이상의 광자를 동시에 흡수하여 얻게 됩니다. 지난 10년 동안, 여러 가지 형광 염료가 등장하며 다광자 이미징 스펙트럼 범위를 (680-1300 nm) 확장시켰습니다. 그림 1 에서 요약된 염료들을 한눈에 확인할 수 있습니다. 염료는 특정 생물학적 과정과 구조를 조사하기 위한 형광 마커로 사용됩니다. 다광자 흡수 과정은 광자의 밀도가 가장 높은 영역과 직접적으로 관련이 있어, 그 결과 발생하는 형광이 초점면에 국한되게 됩니다. 초점면 이외의 형광 신호를 차단하기 위해 기계적 조리개가 필요하지 않으므로 산란과광 손상이 적습니다. 또한, 다광자 이미징은 근적외선 여기 파장을 사용하기 때문에 샘플 내에서 1 mm 이상의 3차원 입체 영상을 생성할 수 있습니다.
다광자 이미징의 진화
1990년대 초부터 타이타늄:사파이어 (Ti:sapphire) 레이저는 다광자 이미징에 선호되는 광원이었습니다. 고체레이저 아키텍쳐는 근적외선 스펙트럼 영역(700 – 1000 nm)에서 견고하며 신뢰성 있는 동작을 제공합니다. 다광자 이미징에 적용했을 때 작업 흡수 영역은 2광자 프로세스의 경우 (~350-500 nm), 3광자 프로세스의 경우 (~233-333 nm)로 변환되며, 이는 생물학적으로 관련이 있는 다양한 형광단에 이상적인 범위입니다.
가장 인기 있는 형광 단백질은 900 nm 이상 파장의 2광자 영역에서 최적으로 여기 됩니다: eGFB (930 nm), eYFP (960 nm) 및 적색 이동 단백질은 mCherry, tdTomato, DSRed, E2-Crimson 과 같이 1000-1100 nm에서 가장 잘 여기 됩니다.
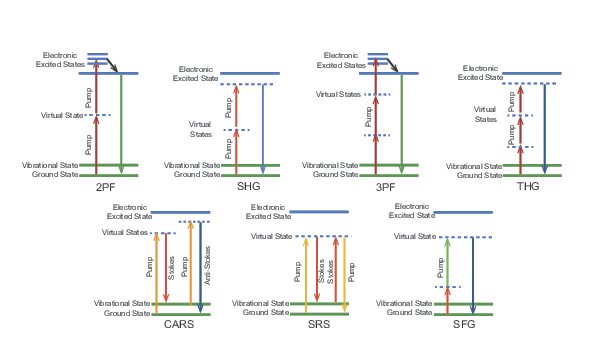
다광자 이미징을 위한 최근 세대의 레이저는 이테르븀(Yb)을 기반으로 합니다. 이 광원들은 비선형 주파수 변환을 사용하여 680 – 1300nm의 범위에서 작동합니다. 이러한 새로운 레이저들은 출력 조절 외에도 고정된 파장의 고출력을 제공하여 second-harmonic generation (SHG), third-harmonic generation (THG), coherent anti-Stokes Raman scattering (CARS) and stimulated Raman scattering (SRS). 과 같은 라벨-프리 기술을 가능하게 합니다. 라벨-프리 방식은 생물학적 샘플에 자연적으로 존재하는 내생적 구조를 드러낼 수 있으며, 함께 사용할 경우, 기존의 다광자 이미징과 결합하면 더 자세한 이미지를 제공합니다. 아래 그림 1을 참조하십시오.
멀티모달 이미징
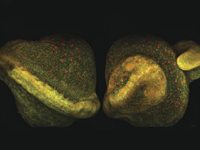
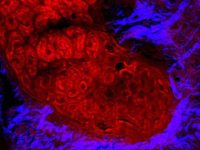
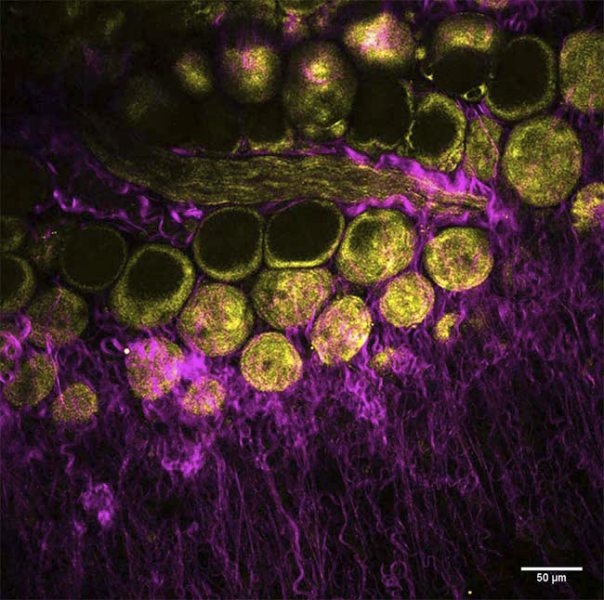
이중 출력 빔을 결합하여 동시 여기를 가능하게 함으로서, 끊임없이 변화하는 멀티모달 이미징의 요구 사항을 충족할 새로운 플랫폼이 준비되었습니다. 파리에 위치한 Curie/CNRS 연구소의 Marie Irondelle 박사는 젖샘 내 종양 발생 원인을 연구합니다 (그림 2 참조). 이전 실험에서는 생쥐의 젖샘을 형광 염료를 사용하지 않고 이미지화했습니다. Irondelle 박사는 SHG 이미징(마젠타색)으로 콜라겐을 THG 이미징(노란색)으로 지방세포를 동시에 관찰했습니다.
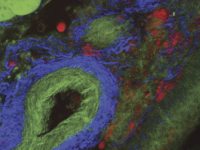
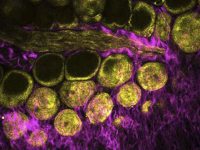
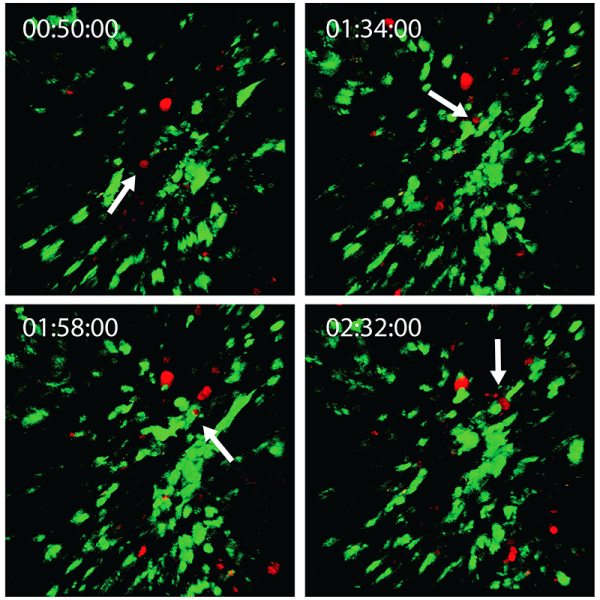
멀티모달 이미징 방식은 생체 내 실험을 수행하는 데 아주 유용할 수 있습니다. 시드니에 있는 100주년 암 의학 및 세포 생물학 연구소의 Michael Kuligowski 박사는 피부에서 T 세포와 수지상세포 사이의 상호 작용을 연구하고 있습니다 (그림 3 참조). 실험에서, CMTPX로 표시된 T 세포를 실험용 생쥐에서 채취하여 GFP로 표시된 수지상세포가 있는 다른 생쥐에 주입했습니다. GFP 라벨이 붙은 수지상세포는 925 nm 에서 튜닝한 Mai Tai® DeepSee™ Ti:sapphire 레이저로 이미징하였고, CMTPX 라벨의 T세포는 1080 nm 에서 튜닝한 InSight® DS+ 로 이미징하였습니다. 실험은 약 40분 동안 수지상세포와 상호작용하는 T 세포만을 관찰합니다.
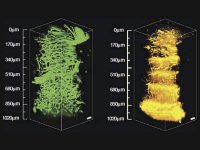
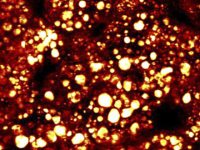
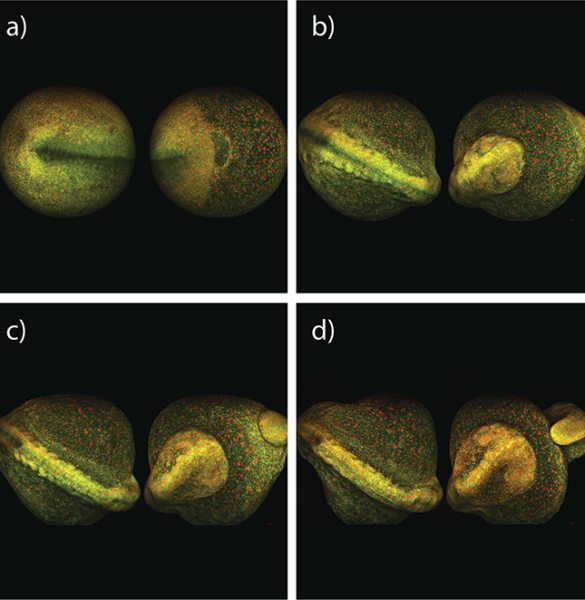
또 다른 실험은 다광자 이미징을 사용하여 전체적인 제브라피시 배아의 초기 발달을 관찰합니다. 아래 그림 4 와 같이 프랑스 Gif-sur-Yvette 에 있는 프랑스 국립 과학 연구 센터의 Nadine Peyrieas 박사는 InSight DS+ Dual을 사용하여 8시간 동안 배아를 관찰했습니다. 레이저의 이중 빔 구성을 사용하여 980 nm 와 1041 nm 에서 동시에 다광자 이미징이 가능했습니다. 배아 세포막은 eGFP로, 세포 핵은 mCherry 로 표시되었습니다.
전체적인 제브라피쉬 배아의 초기 발달은 감소된 전력 수준에서 MPEF 현미경을 사용하여 연속적으로 영상화할 수 있습니다. 이 실험에서, Nadine Peyrieas 박사는 InSight DS+ Dual 이 장착된 현미경을 사용하여 8시간 동안 배아의 발달을 관찰했습니다(그림 4 참조). 배아 세포막은 eGFP로, 세포 핵은 mCherry로 표시되었습니다. 레이저의 이중 빔 구성을 사용하여 eGFP 와 mCherry 를 각각 980 nm 와 1041 nm 에서 동시에 이미지화했습니다. 배아는 앞면과 뒷면 모두에서 순차적으로 이미지화되었습니다.
다광자 이미징 기술